 Back
BackStruktur Atom: Teori, Partikel Dasar, Konfigurasi Elektron, dan Sifat Periodik
Study Guide - Smart Notes

Struktur Atom
Perkembangan Teori Atom
Studi tentang struktur atom merupakan fondasi utama dalam ilmu kimia, karena atom adalah bagian terkecil dari materi yang terdiri dari proton, neutron, dan elektron. Berbagai teori dan eksperimen telah dikembangkan untuk memahami bagaimana atom tersusun dan bagaimana sifat-sifat materi ditentukan oleh partikel-partikel tersebut.
Teori Unsur Kuno: Filsuf Yunani seperti Thales, Anaximenes, Heraklitus, dan Empedocles mengemukakan bahwa materi terdiri dari unsur-unsur sederhana seperti air, udara, api, dan tanah.
Teori Atomistik: Democrites dan Leukippes memperkenalkan gagasan bahwa materi tersusun dari partikel kecil yang tidak dapat dibagi lagi, disebut atom.
Hukum Kekekalan Massa: Antoine Lavoisier membuktikan bahwa massa dalam sistem tertutup tetap konstan selama reaksi kimia.
Hukum Komposisi Konstan: Joseph Proust menyatakan bahwa senyawa murni selalu memiliki perbandingan massa unsur yang tetap.
Hukum Perbandingan Berganda: John Dalton menunjukkan bahwa unsur-unsur membentuk senyawa dengan perbandingan massa bilangan bulat kecil.






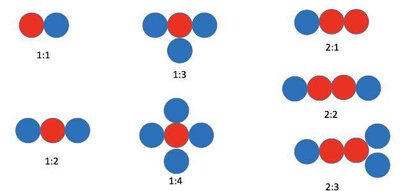

Teori Atom Dalton
Dalton mengemukakan bahwa atom adalah partikel terkecil yang tidak dapat dibagi, dan atom dari unsur yang sama memiliki sifat identik. Senyawa terbentuk dari penggabungan atom-atom dalam perbandingan bilangan bulat kecil.
Atom tidak dapat diuraikan menjadi partikel lebih kecil.
Atom dari unsur yang sama identik.
Atom dari unsur berbeda memiliki sifat berbeda.
Senyawa terbentuk dari penggabungan atom.

Teori Atom Thomson
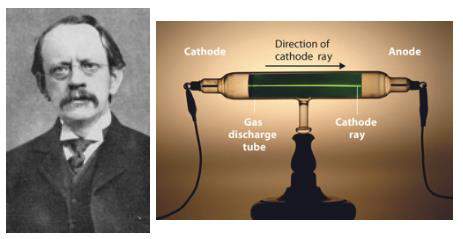
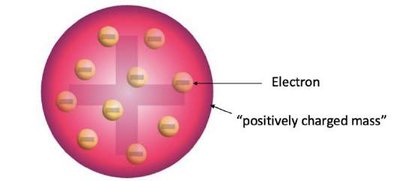
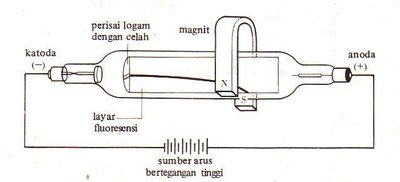
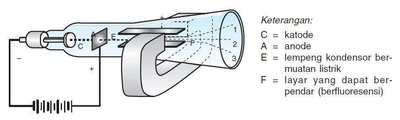
Thomson menemukan elektron melalui eksperimen sinar katoda dan mengembangkan model atom "puding plum", di mana elektron tertanam dalam massa bermuatan positif.
Penemuan elektron: Sinar katoda terdiri dari partikel bermuatan negatif.
Model atom puding plum: Elektron tersebar dalam bola bermuatan positif.

Partikel Dasar Atom
Atom terdiri dari tiga partikel dasar: elektron, proton, dan neutron. Masing-masing memiliki sifat dan peran yang berbeda dalam menentukan sifat atom.
Elektron: Bermuatan negatif, massa sangat kecil, ditemukan melalui sinar katoda.
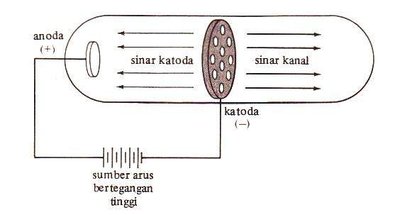
Proton: Bermuatan positif, massa lebih besar dari elektron, ditemukan melalui sinar kanal.
Neutron: Tidak bermuatan, massa hampir sama dengan proton, ditemukan oleh Chadwick.
Nama | Lambang | Massa (gr) | Massa (sma) | Muatan |
|---|---|---|---|---|
Proton | p+ | 1,6726 x 10-24 | 1,0078 | +1 |
Neutron | n | 1,6749 x 10-24 | 1,0087 | 0 |
Elektron | e- | 9,1096 x 10-28 | 5,4859 x 10-4 | -1 |
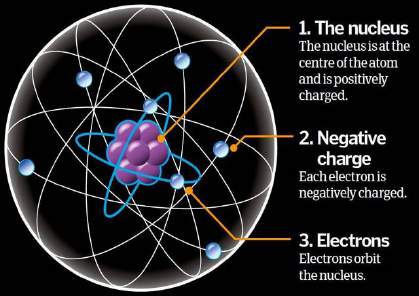
Teori Atom Rutherford
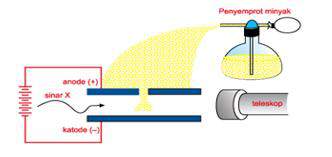
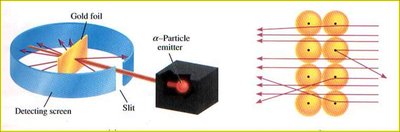
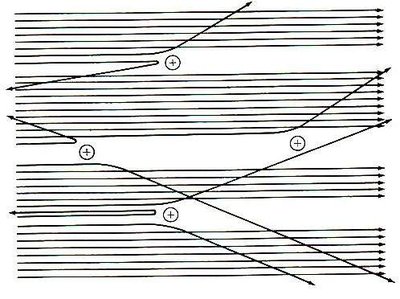
Rutherford melakukan eksperimen hamburan partikel alfa pada lempeng emas dan menemukan bahwa atom memiliki inti kecil bermuatan positif yang dikelilingi oleh elektron.
Inti atom: Massa dan muatan positif terkonsentrasi di inti.
Elektron: Beredar mengelilingi inti pada jarak relatif jauh.

Teori Atom Bohr
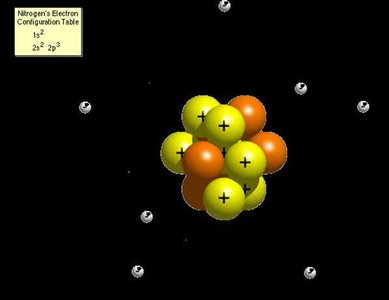
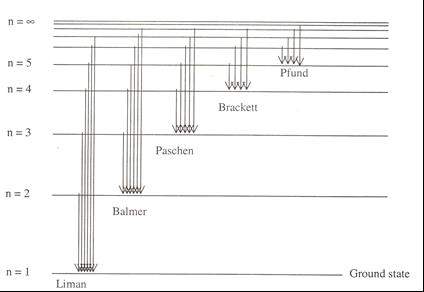
Niels Bohr memperbaiki model Rutherford dengan teori kuantum, menyatakan bahwa elektron mengelilingi inti dalam lintasan tertentu (orbit) dan hanya dapat berpindah antar lintasan dengan menyerap atau memancarkan energi.
Orbit elektron: Elektron bergerak dalam lintasan lingkaran dengan energi tertentu.
Energi diskrit: Perubahan energi terjadi saat elektron berpindah lintasan.
Persamaan energi:

Teori Atom Mekanika Gelombang
Louis de Broglie, Heisenberg, dan Schödinger mengembangkan mekanika kuantum, yang menyatakan bahwa elektron memiliki sifat gelombang dan partikel. Prinsip ketidakpastian Heisenberg menyatakan posisi dan momentum elektron tidak dapat ditentukan secara simultan dengan akurat.
Persamaan de Broglie:
Prinsip ketidakpastian:
Persamaan gelombang Schödinger: Digunakan untuk menentukan energi dan posisi elektron dalam atom.

Bilangan Kuantum
Setiap elektron dalam atom memiliki empat bilangan kuantum yang menentukan posisi dan sifatnya:
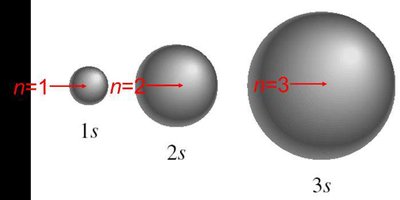
Bilangan kuantum utama (n): Menunjukkan tingkat energi utama.
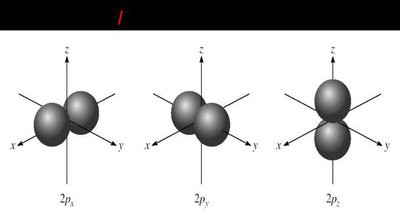
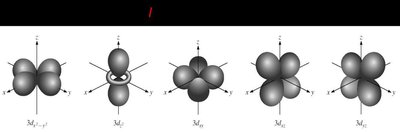
Bilangan kuantum azimut (l): Menunjukkan sub tingkat energi dan bentuk orbital.
Bilangan kuantum magnetik (m): Menunjukkan orientasi orbital.
Bilangan kuantum spin (s): Menunjukkan arah rotasi elektron.
Konfigurasi Elektron
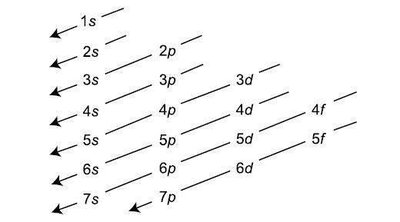
Konfigurasi elektron adalah susunan elektron dalam orbital atom. Pengisian elektron mengikuti aturan Aufbau, Hund, dan larangan Pauli.
Aturan Aufbau: Elektron mengisi orbital dengan energi terendah terlebih dahulu.
Aturan Hund: Elektron cenderung tidak berpasangan dalam orbital yang sama.
Larangan Pauli: Tidak ada dua elektron dalam satu atom yang memiliki keempat bilangan kuantum yang sama.
Sub kulit | Jumlah Orbital | Elektron maksimum |
|---|---|---|
s | 1 | 2 |
p | 3 | 6 |
d | 5 | 10 |
f | 7 | 14 |
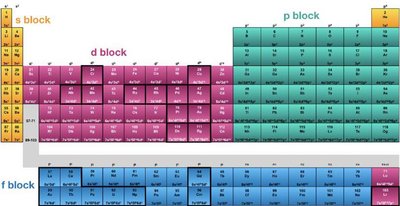
Sifat Periodik Atom
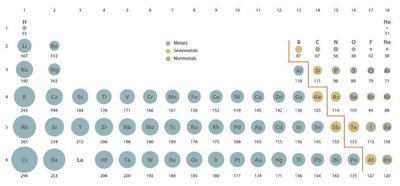
Tabel periodik unsur mengurutkan unsur berdasarkan nomor atom dan sifat periodik. Sifat periodik meliputi jari-jari atom, energi ionisasi, afinitas elektron, dan keelektronegatifan.
Jari-jari atom: Menurun dari kiri ke kanan dalam satu periode.
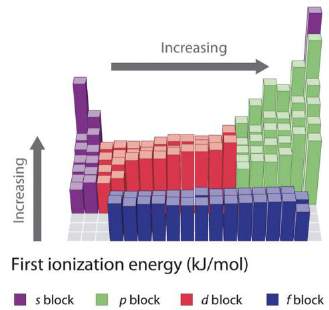
Energi ionisasi: Energi yang dibutuhkan untuk melepaskan elektron dari atom netral, meningkat dari kiri ke kanan.
Afinitas elektron: Energi yang dilepaskan atau dibutuhkan saat menambah elektron ke atom netral.
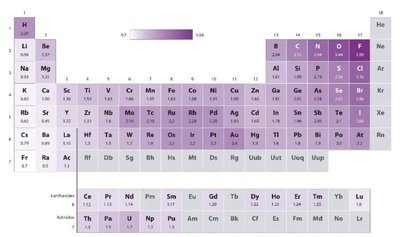
Keelektronegatifan: Kemampuan atom menarik elektron dalam ikatan kimia.
Soal Latihan
Jelaskan sumbangan Thomson, Rutherford, Bohr, dan de Broglie terhadap struktur atom.
Bandingkan model atom Rutherford dan Bohr.
Hitung panjang gelombang proton dengan kecepatan 1,3 x 107 m/s dan massa 1,67 x 10-24 g.
Mengapa jumlah proton dan elektron harus sama dalam atom?
Tentukan jumlah proton, elektron, dan neutron dari 23Na dan 39K.
Sebutkan bilangan kuantum orbital 2p.
Tentukan kemungkinan keempat bilangan kuantum untuk n=5, l=0 dan n=4, l=1.
Tentukan harga bilangan kuantum elektron terakhir untuk 11Na, 16S, dan 28Ni.
Tentukan konfigurasi elektron dari 20Ca, 35Br, 47Ag, 58Ce, 86Rn, dan 91Pa.
Berapakah jumlah elektron yang dapat dipunyai atom dengan bilangan kuantum n=2, l=1; n=3, l=0; n=3, l=2, m1=-1?
Tentukan susunan elektron pada keadaan dasar dari atom 8O, 11Na, 12Mg, 20Ca, 24Cr.
Berapakah jumlah elektron tidak berpasangan pada atom 14Si dan 29Cu?
