 Back
BackConceptos Básicos de Materia y Estructura Atómica: Propiedades Periódicas, Enlaces y Estructuras de Lewis
Study Guide - Smart Notes

Unidad 1: Conceptos Básicos de Materia y Estructura Atómica
Clasificación y Propiedades Periódicas de los Elementos
La tabla periódica organiza los elementos según sus propiedades químicas y electrónicas, permitiendo identificar tendencias periódicas como electronegatividad, tipos de elementos y bloques.
Metales: Tienden a ceder electrones y formar cationes.
No metales: Tienden a ganar electrones y formar aniones.
Metaloides: Presentan propiedades intermedias entre metales y no metales.
Bloques: s, p, d, f, según el orbital de mayor energía ocupado por electrones.
Tipo de Elemento | Propiedad |
|---|---|
Metales | Ceden electrones |
No metales | Ganan electrones |
Metaloides | Propiedades mixtas |
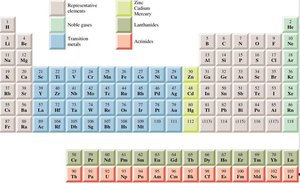
Los elementos se agrupan en grupos (columnas) y periodos (filas). Los elementos de un mismo grupo tienen configuraciones electrónicas similares y propiedades análogas.
Propiedades Periódicas: Electronegatividad
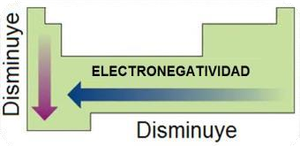
Electronegatividad (E.N) es la capacidad de un átomo para atraer electro nes en un enlace químico. Esta propiedad varía a lo largo de la tabla periódica:
Aumenta de izquierda a derecha en un periodo.
Disminuye de arriba hacia abajo en un grupo.
El elemento más electronegativo es el Flúor (F) con E.N = 4.0; los menos electronegativos son Cesio (Cs) y Francio (Fr) con E.N ≈ 0.7.

Elemento | Electronegatividad |
|---|---|
Flúor (F) | 4.0 |
Cesio (Cs) | 0.7 |
Francio (Fr) | 0.7 |

Número de Oxidación
El número de oxidación es la carga que queda en un elemento dentro de un compuesto si los electrones del enlace se asignan al átomo más electronegativo. Es fundamental para entender la reactividad y la formación de compuestos.
Tipos de Enlaces Químicos
Enlace Iónico
El enlace iónico se forma cuando un átomo transfiere electrones a otro, generando iones de carga opuesta que se atraen electrostáticamente. Ocurre entre metales (grupos IA, IIA) y no metales (grupos VIA, VIIA) con diferencia de electronegatividad ΔE.N ≥ 1.7.
Se forman sólidos cristalinos con altos puntos de fusión.
En estado sólido no conducen electricidad, pero sí en solución acuosa o fundidos.


Enlace Covalente
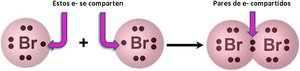
El enlace covalente implica la compartición de electrones entre átomos. Puede ser apolar o polar según la diferencia de electronegatividad.
Covalente apolar: ΔE.N = 0, átomos idénticos o de igual electronegatividad (ejemplo: H2, Cl2).
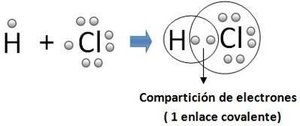
Covalente polar: 0 < ΔE.N ≤ 1.7, átomos diferentes (ejemplo: HCl).
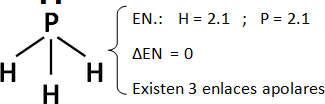
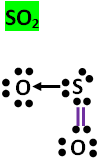
Enlace Covalente Dativo (Coordinado)
En el enlace covalente dativo, un solo átomo aporta ambos electrones para el enlace. Se representa con una flecha y es común en moléculas como HNO3 y SO2.


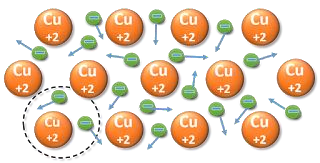
Enlace Metálico
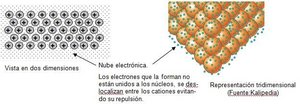
El enlace metálico es la fuerza de atracción entre cationes metálicos y una nube de electrones deslocalizados. Explica propiedades como conductividad eléctrica y maleabilidad en metales.

Estructuras de Lewis y la Regla del Octeto
Estructuras de Lewis
Las estructuras de Lewis representan los electrones de valencia como puntos alrededor del símbolo del elemento. Permiten visualizar la formación de enlaces y pares libres.
Regla del Octeto y Excepciones
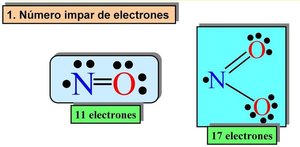
La regla del octeto establece que los átomos tienden a rodearse de ocho electrones de valencia. Existen excepciones, como el dueto para el hidrógeno y casos donde el octeto se expande o no se completa.
Dueto: Hidrógeno y helio se estabilizan con dos electrones.
Menos de un octeto: Compuestos de Be y B.
Octeto expandido: Elementos como S y P pueden tener más de ocho electrones.

Excepción | Ejemplo |
|---|---|
Dueto | H2, He |
Menos de octeto | BeH2, BH3 |
Octeto expandido | SF6, PF5 |
Cálculo de Carga Formal
La carga formal ayuda a determinar la estructura de Lewis más estable. Se calcula como:
Fórmula:
La suma de las cargas formales debe igualar la carga total de la molécula o ion.
Ejemplo: En CO2, la carga formal de cada átomo es cero, lo que indica una estructura estable.
Resumen de Conceptos Clave
La tabla periódica permite clasificar elementos y predecir propiedades.
Electronegatividad es fundamental para entender la formación de enlaces.
Existen diferentes tipos de enlaces: iónico, covalente (apolar, polar, dativo) y metálico.
Las estructuras de Lewis y la regla del octeto ayudan a visualizar la distribución de electrones y la estabilidad de moléculas.
Las excepciones a la regla del octeto son importantes para comprender la química de elementos ligeros y pesados.
Bibliografía recomendada: Jones, Principios de Química; Atkins; Brown, Química La ciencia central; Phillips Stropzak Wistrom, Química Conceptos Aplicaciones.
